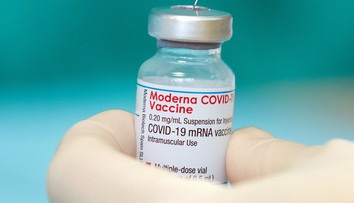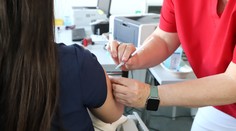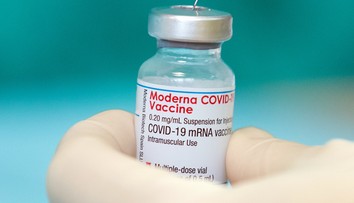
Máme druhú vakcínu proti koronavírusu! Je od firmy Moderna a ľahšie sa skladuje
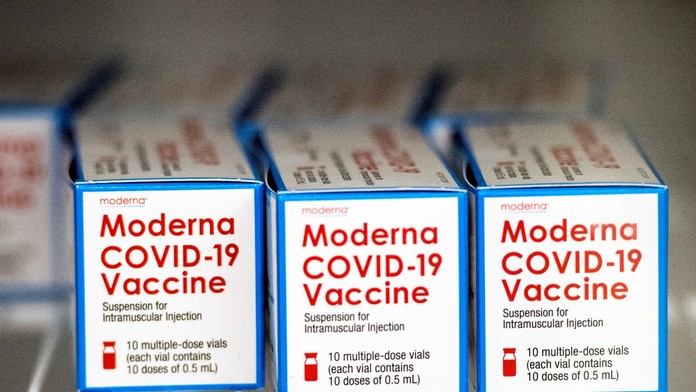
Vakcínu popoludní schválila na použitie v Únii aj Európska komisia
Európska lieková agentúra (EMA) odporučila udelenie podmienečnej registrácie pre druhú vakcínu na prevenciu ochorenia COVID-19: COVID-19 Vakcína Moderna. Vakcína je určená pre dospelých od 18 rokov a spĺňa všetky požiadavky na bezpečnosť, účinnosť a kvalitu vakcín platné v Európskej únii.
Európska komisia v stredu popoludní vydala podmienené povolenie na uvedenie na trh pre vakcínu proti COVID-19 vyvinutú spoločnosťou Moderna. Komisia spresnila, že povolenie je v súlade s pozitívnym vedeckým odporúčaním založeným na dôkladnom posúdení bezpečnosti, účinnosti a kvality vakcíny zo strany Európskej agentúry pre lieky (EMA) a je schválené členskými štátmi EÚ.
Komisia pripomenula, že ide v poradí o druhú vakcínou proti ochoreniu COVID-19 povolenú na trhu EÚ.
Predsedníčka EK Ursula von der Leyenová v tejto súvislosti uviedla, že s vakcínou Moderna budú mať občania EÚ k dispozícii ďalších 160 miliónov dávok očkovacích látok. "A ďalšie vakcíny prídu. Európa zabezpečila až dve miliardy dávok potenciálnych vakcín proti COVID-19. Budeme mať viac ako dosť bezpečných a účinných vakcín na ochranu všetkých Európanov," odkázala v správe pre médiá.
Podľa vysvetlenia eurokomisárky pre zdravie a bezpečnosť potravín Stelly Kyriakidisovej EÚ dojednala najširšie portfólio vakcín na svete pre všetky svoje členské štáty. Komisárka spresnila, že povolením druhej bezpečnej vakcíny, od spoločnosti Moderna, sa spolu s vakcínou od konzorcia BioNTech/Pfizer zabezpečí, že EÚ bude mať k dispozícii 460 miliónov dávok, a ďalšie prídu "s rastúcou rýchlosťou".
"Členské štáty musia teraz zabezpečiť správne tempo očkovania. Naše úsilie sa nezastaví, kým nebudú vakcíny dostupné pre všetkých v EÚ," povedala komisárka.
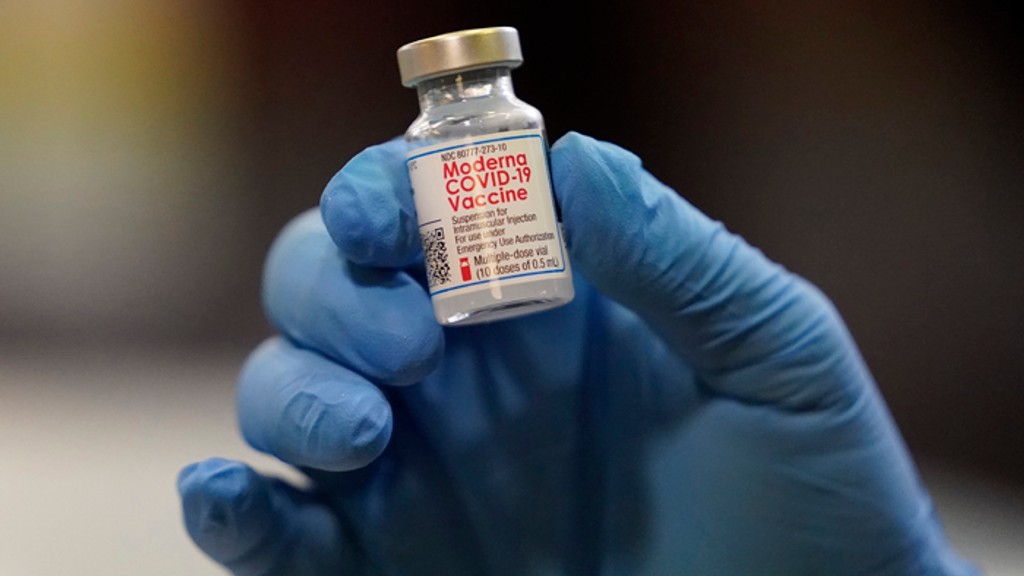
Rozsiahle klinické skúšania preukázali, že vakcína COVID-19 Vakcína Moderna je účinná pri prevencii ochorenia COVID-19 u ľudí od 18 rokov. Klinické skúšanie zahŕňalo približne 30 000 ľudí, ktorí boli rozdelení do dvoch skupín. Polovica dostala vakcínu a polovica placebo, pričom skúšanie bolo zaslepené, t.j. účastníci neboli informovaní, do ktorej skupiny patria.
Samotná účinnosť bola určená v III. fáze klinického skúšania v skupine 28 000 ľudí od 18 do 94 rokov, u ktorých predtým nebolo potvrdené ochorenie COVID-19. Skúšanie ukázalo, že vakcína znížila počet symptomatických prípadov COVID-19 o 94,1 %: v skupine, ktorá dostala vakcínu sa vyskytlo 11 prípadov nákazy (zo 14 134 účastníkov), v skupine s placebom 185 prípadov (zo 14 073 účastníkov). To znamená, že vakcína v klinickom skúšaní preukázala účinnosť 94,1 %.
U účastníkov, u ktorých je vyššie riziko závažného priebehu ochorenia COVID-19 (vrátane pacientov s chronickým ochorením pľúc, ochoreniami srdca, obezitou, ochoreniami pečene, diabetom a HIV), sa preukázala účinnosť 90,9 %. Vysoká účinnosť bola potvrdená bez ohľadu na pohlavie či rasovú alebo etnickú príslušnosť.
Vakcína sa podáva v dvoch dávkach do ramena, pričom odstup medzi dávkami je 28 dní. Najčastejšie nežiaduce účinky po očkovaní danou vakcínou sú zvyčajne mierne a krátkodobé. Patria k nim bolesť a začervenanie v mieste vpichu, napuchnuté alebo citlivé uzliny v podpazuší, únava, bolesť hlavy, svalov a kĺbov, zimnica, horúčka, nevoľnosť a zvracanie.
Účinnosť a bezpečnosť vakcíny sa bude naďalej monitorovať prostredníctvom farmakovigilančných systémov v jednotlivých členských štátoch, v Európskej únii a prostredníctvom dodatočných postregistračných štúdií.
Európska komisia bezodkladne posúdi stanovisko Európskej liekovej agentúry a vydá rozhodnutie o registrácii. Takéto rozhodnutie je automaticky platné vo všetkých členských štátoch Európskej únie.
Komu je a nie je vakcína určená
Vakcína je určená pre dospelých od 18 rokov.
Vakcína sa nemá podávať ľuďom alergickým na niektorú jej zložku.
Informácie o použití vakcíny u osobitných skupín pacientov vrátane tehotných a dojčiacich žien sú súčasťou informácií o lieku (PIL, SPC).
Ak EK vydá rozhodnutie o registrácii, bude platné v celej EÚ
Ak Európska komisia vydá rozhodnutie o registrácii novej vakcíny na prevenciu ochorenia COVID-19 od spoločnosti Moderna, bude automaticky platné vo všetkých členských štátoch EÚ. "Európska komisia bezodkladne posúdi stanovisko EMA a vydá rozhodnutie o registrácii," spresnila Štátneho ústavu pre kontrolu liečiv Magdaléna Jurkemíková.

Podmienečná registrácia znamená, že v čase vydania registračného rozhodnutia žiadateľ nedodal údaje o účinnosti a bezpečnosti lieku v takom rozsahu, ako sa štandardne vyžaduje. "Aj v takomto prípade musia prínosy lieku prevažovať nad potenciálnymi rizikami spojenými s neúplnými údajmi," zdôraznila.
Podľa jej slov aj pri podmienečnej registrácii musí byť dostatočne preukázaná bezpečnosť, kvalita a účinnosť vakcíny. Klinické skúšanie zahŕňalo približne 30-tisíc ľudí.
Celé Televízne noviny nájdete na markizaplus.sk.
Práve sa číta
Sledujte Televízne noviny vo full HD a bez reklám na Voyo